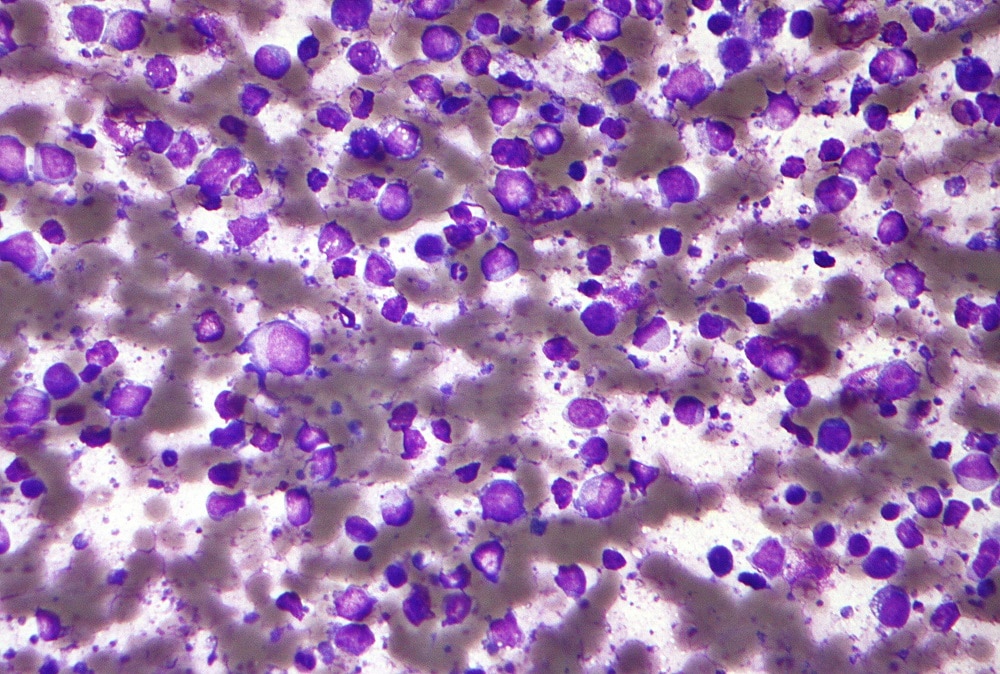
- Новый таргетный препарат продемонстрировал улучшение клинических результатов у пациентов с рецидивирующей или рефрактерной диффузной B-крупноклеточной лимфомой по сравнению со стандартной терапией.
- Это первый в своем классе конъюгат антитело-препарат, нацеленный на белок CD79b, экспрессируемый большинством B-клеток.
- В портфеле гематологических препаратов компании «Рош» это уже девятое показание со статусом «прорыв в терапии» от FDA.
Москва, 3 июля 2019 г. — Компания «Рош» сообщила, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило по ускоренной процедуре заявку на регистрацию препарата полатузумаб ведотин (Polivy™) в комбинации с препаратами бендамустин и ритуксимаб (комбинация BR) для лечения взрослых пациентов с рецидивирующей или рефрактерной (р/р) диффузной B-крупноклеточной лимфомой (ДВКЛ), ранее уже получивших не менее двух вариантов терапии. Данное показание было одобрено по ускоренной процедуре на основе результатов по полному ответу, полученных в рандомизированном контролируемом клиническом исследовании. Программа FDA по ускоренному рассмотрению предусматривает выдачу условного разрешения на применение препаратов, направленных на удовлетворение актуальных медицинских потребностей в лечении тяжелых заболеваний. Дальнейшее утверждение этого показания будет зависеть от верификации и описания клинических преимуществ в подтверждающем исследовании.
«Несмотря на значительный прогресс в лечении диффузной B-крупноклеточной лимфомы, выбор вариантов терапии для рефрактерной или рецидивирующей форм заболевания, после применения нескольких схем лечения, по-прежнему остается очень ограниченным, — говорит д-р Сандра Хорнинг, главный медицинский директор и глава глобального подразделения по разработке лекарственных препаратов “Рош”. — Нынешнее одобрение комбинации с полатузумаб ведотином позволит ускорить доступ к новому варианту терапии для людей с этим агрессивным заболеванием».
Ускоренное одобрение препарата полатузумаб ведотин основано на результатах клинического исследования фазы Ib/II GO29365. Это первое и единственное рандомизированное исследование, которое показало более высокий уровень ответа по сравнению с комбинацией BR (обычно используемый режим) у пациентов с р/р ДВККЛ, которым не показана трансплантация гемопоэтических стволовых клеток. Результаты исследования показали, что 40% участников, получавших полатузумаб ведотин плюс BR достигли полного ответа (n=16/40; 95% CI: 25-57), так что на момент оценки заболевание у них не обнаруживалось, по сравнению с 18% пациентов в группе, где применялась только комбинация BR (n=7/40; 95% CI: 7-33). Показатели частоты полного ответа оценивались независимым наблюдательным комитетом. Исследование также показало, что 45% пациентов, получавших полатузумаб ведотин плюс BR, достигли объективного ответа на конец лечения (n=18/40; 95% CI: 29-62), по сравнению с 18% пациентов, получавших только BR (n=7/40; 95% CI: 733). Из тех, кто получал полатузумаб ведотин плюс BR и достиг полного или частичного ответа, у 64% (n=16/25) длительность ответа (ДО) составила не менее шести месяцев по сравнению с 30% (n=3/10) пациентов, получавших только BR. Кроме того, у 48% (n=12/25) пациентов в группе полатузумаб ведотин плюс BR показатель длительности ответа составил не менее года, по сравнению с 20% (n=2/10) пациентов с таким же результатом из тех, кто получал только BR. Нежелательные явления, наблюдавшиеся не менее чем у 20% пациентов и при этом, как минимум, на 5% чаще у пациентов в группе полатузумаба ведотина плюс BR по сравнению с BR, включали низкий уровень лейкоцитов, тромбоцитов и эритроцитов, онемение, покалывание или боль в руках и ногах, диарею, лихорадку, снижение аппетита и пневмонию.
FDA предоставило право на приоритетное рассмотрение заявке «Рош» на регистрацию биопрепарата полатузумаб ведотин в феврале 2019 года. FDA предоставляет право на приоритетное рассмотрение препаратам, которые, по мнению Управления, способны обеспечить значительные улучшения в плане безопасности и эффективности при лечении, профилактике или диагностике серьезных заболеваний. Кроме того, полатузумаб ведотин также получил статус «прорыв в терапии» от FDA и включен в программу по приоритетным препаратам PRIME (PRIority MEdicines) Европейского агентства по лекарственным средствам (EMA) для лечения пациентов с р/р ДВКЛ в 2017 году. Статус «прорыв в терапии» предназначен для ускорения разработки и одобрения лекарственных препаратов, предназначенных для лечения серьезных заболеваний, при наличии предварительных доказательств того, что они могут обеспечить существенные улучшения результатов лечения по сравнению с существующими методами.
Об исследовании GO29365
GO29365 — международное исследование фазы Ib/II по оценке безопасности, переносимости и активности полатузумаба ведотина в комбинации с препаратами ритуксимаб или обинутузумаб и бендамустин при рецидивирующей или рефрактерной (р/р) фолликулярной лимфоме или диффузной В-крупноклеточной лимфоме (ДБКЛ). Пациенты, подходящие для включения в исследование, не являлись кандидатами для трансплантации гемопоэтических стволовых клеток на момент включения. В исследовании фазы II 80 пациентов с р/р ДБКЛ, ранее уже получивших интенсивное лечение, были рандомизированы для получения комбинации бендамустин плюс ритуксимаб (BR), или BR в комбинации с полатузумабом ведотином в течение фиксированного интервала времени — шести циклов длительностью 21 день каждый. До участия в исследовании пациенты получили в среднем две линии терапии (от 1 до 7 в группе с полатузумабом ведотином, от 1 до 5 в группе BR). Первичной конечной точкой был полный ответ (ПО) на момент завершения лечения по результатам позитронно-эмиссионной томографии (ПЭТ) по оценке независимого наблюдательного комитета (ННК). Остальные ключевые конечные точки включали частоту объективного ответа (ЧОО: полный и частичный ответ) по оценке исследователей и наилучший объективный ответ по окончанию лечения по оценке исследователей и ННК. Конечные точки включали в себя длительность ответа, выживаемость без прогрессирования заболевания (ВБП), бессобытийную выживаемость и общую выживаемость.
О препарате полатузумаб ведотин-piiq
Полатузумаб ведотин (Polivy™) — это первый в своем классе конъюгат анти-CD79b антитела и лекарственного препарата (ADC). Белок CD79b является высокоспецифичным и экспрессируется при большинстве типов B-клеточных неходжскинских лимфом (НХЛ), поэтому он является перспективной мишенью при разработке новых препаратов1. Полатузумаб ведотин связывается с CD79b, инициируя интернализацию терапевтического средства в клетку. При этом химиотерапевтическое средство (монометилауристатин Е (ММАЕ), которое связано с моноклональным антителом) попадает в В-клетку. Считается, что благодаря такому процессу достигается максимальная гибель опухолевых клеток, в то время как воздействие на нормальные клетки сводится к минимуму2. Препарат полатузумаб ведотин разрабатывается компанией «Рош» с помощью технологии Seattle Genetics ADC и в настоящее время исследуется для лечения нескольких типов НХЛ.
О диффузной B-крупноклеточной лимфоме
Диффузная В-крупноклеточная лимфома (ДБКЛ) — наиболее распространенный подтип неходжкинской лимфомы (НХЛ), встречающийся примерно в каждом третьем случае НХЛ3. ДБКЛ — это агрессивный (быстро развивающийся) тип НХЛ, при котором ответ на терапию обычно достигается в первой линии4. Однако примерно у 40% пациентов возникает рецидив, после чего варианты терапии спасения ограничены, а продолжительность жизни значительно сокращается5 Ежегодно в мире диагностируется около 150 тысяч случаев заболевания ДВКЛ6.
«Рош» в гематологии
Более 20 лет компания «Рош» занимается разработкой инновационных лекарственных препаратов, которые обеспечивают значительный прогресс в лечении злокачественных и незлокачественных гематологических заболеваний. Компания обладает обширными знаниями и опытом в этой терапевтической области. В настоящее время «Рош» прикладывает большие усилия и инвестирует в разработку инновационных способов лечения пациентов, страдающих гематологическими заболеваниями. К нашим зарегистрированным препаратам относятся ритуксимаб (торговая марка Мабтера®), обинутузумаб (Газива®), полатузумаб ведотин (Polivy™), венетоклакс (Венклекста) (в сотрудничестве с компанией AbbVie) и эмицизумаб (Гемлибра). Портфель исследуемых лекарственных препаратов для лечения онкогематологических заболеваний включает идасанутлин – малую молекулу – антагонист взаимодействия MDM2 с p53, биспецифические антитела с участием Т-клеток, нацеленные на CD20 и CD3, а также атезолизумаб (Тецентрик®), моноклональное антитело, предназначенное для связывания с PD-L1. Наш научный опыт, в сочетании с широким портфелем и линейкой перспективных препаратов, предоставляют уникальную возможность для разработки комбинированных режимов терапии, направленных на дальнейшее улучшение жизни пациентов.
Все торговые марки, используемые или упомянутые в этом сообщении, защищены законом.
- Dornan D, et al. Therapeutic potential of an anti-CD79b antibody-drug conjugate, anti-CD79b-vc-MMAE, for the treatment of non-Hodgkin lymphoma. Blood 2009; 114:2721-2729. Pfeifer M, et al. Anti-CD22 and anti-CD79B antibody drug conjugates are active in different molecular diffuse large B-cell lymphoma subtypes. Leukemia 2015; 29:1578-1586.
- Ducry L, Stump B. Antibody-drug conjugates: linking cytotoxic payloads to monoclonal antibodies. Bioconjug Chem. 2010; 21:5 — 13. ADC Review. What are antibody-drug conjugates? [Интернет; июнь 2019 г.]. Доступно по ссылке: https://adcreview.com/adc-university/adcs-101/antibody-drug-conjugates-adcs/.
- Lyon, France. World Health Organization Classification of Tumors of Haematopoietic and Lymphoid Tissues. IARC Press; 2008.
- Maurer, JM et al. Event-free survival at 24 months is a robust end point for disease-related outcome in diffuse large B-cell lymphoma treated with immunochemotherapy. J Clin Oncol 2014; 32:1066-73.
- Dornan D, et al. Therapeutic potential of an anti-CD79b antibody-drug conjugate, anti-CD79b-vc-MMAE, for the treatment of non-Hodgkin lymphoma. Blood 2009; 114:2721-2729. ADC Review. What are antibody-drug conjugates? [Интернет; июнь 2019 г.]. Доступно по ссылке: https://adcreview.com/adc-university/adcs-101/antibody-drug-conjugates-adcs/.
- Numbers derived from GLOBOCAN 2018: Estimated cancer incidence, mortality and prevalence worldwide in 2018. [Интернет; июнь 2019 г.]. Доступно по ссылке: http://globocan.iarc.fr.











































Odnoklassniki
VKontakte
Telegram
RSS