Ревматоидный артрит — что это такое?
Ревматоидный артрит — это хроническое аутоиммунное заболевание, при котором поражение сустава опосредовано цитокинами, хемокинами и металлопротеиназами. Характерно воспаление симметричных периферических суставов (например, суставов запястья, плюснефаланговых), часто приводящее к прогрессирующей деструкции суставных структур; при этом также наблюдаются признаки системного поражения. Диагностика проводится при анализе специфических клинических проявлений, результатов лабораторных и рентгенологических исследований. При лечении используются лекарственные средства, физиотерапия, в некоторых случаях — хирургические методы. Лекарственная терапия сводится к комбинации НПВП (помогающих снизить выраженность симптоматики) и базисных противоревматических препаратов, которые замедляют прогрессирование заболевания.
Ревматоидный артрит встречается в популяции с частотой приблизительно 1 %. Заболеваемость среди женщин в 2—3 раза выше, чем у мужчин. Болезнь может манифестировать в любом возрасте, но наиболее часто заболевают лица в возрасте от 35 до 50 лет. Могут также болеть дети и лица пожилого возраста.
Этиология, патофизиология
Несмотря на то что ревматоидный артрит опосредован аутоиммунными реакциями, точная причина заболевания неизвестна; многие факторы могут вносить свой вклад в его развитие. Доказана генетическая предрасположенность к заболеванию: в европеоидной популяции она связана с эпитопом β1 локуса HLA-DR II класса антигенов гистосовместимости. Факторы окружающей среды (например, вирусные инфекции) и курение, возможно, также играют определенную роль.
Основные нарушения со стороны иммунной системы включают продукцию иммунных комплексов линиями клеток синовиальной мембраны и воспаленных кровеносных сосудов. Плазматические клетки продуцируют антитела [например, ревматоидный фактор (РФ)], которые также способствуют образованию этих комплексов. На ранних стадиях заболевания макрофаги мигрируют в пораженную синовиальную оболочку; повышенное количество воспалительных клеток макрофагального происхождения характерно для воспаления сосудов. Т-лимфоциты, инфильтрирующие синовиальную ткань, имеют фенотип CD4+ Макрофаги и лимфоциты, инфильтрирующие синовиальную оболочку, продуцируют провоспали-тельные цитокины и хемокины [например, фактор некроза опухоли (ФИО), колониестимулирующий фактор гранулоцитов и макрофагов, различные интерлейкины (ИЛ) и гамма-интерферон]. Выброс медиаторов воспаления, вероятно, приводит к развитию суставных и системных проявлений ревматоидного артрита.
При хроническом поражении в норме тонкая и нежная синовиальная мембрана значительно утолщается, образуя множественные ворсиноподобные складки. Кроме того, клетки синовия продуцируют ряд веществ, включая коллагеназу и стромелизин (которые вызывают деструкцию хрящевой ткани), ИЛ-1, ФНО-а (которые стимулируют деструкцию хряща и резорбцию кости, опосредованную остеокластами, и воспаление синовиальной оболочки) и простагландины (которые потенцируют воспаление). Имеют место отложения фибрина, фиброз и некроз. Под действием воспалительных медиаторов развивается гиперпластическая синовиальная ткань (паннус), разрушающая хрящ, субхондральную костную ткань, капсулу сустава и связки. В синовиальной жидкости обнаруживается большое количество полиморфноядерных клеток.
Ревматоидные узелки развиваются у 30 % больных ревматоидным артритом. Они представляют собой гранулемы, состоящие из центральной некротической части, окруженной слоем гистиоцитов (тканевых макрофагов); этот комплекс, в свою очередь, окружен лимфоцитами, плазматическими клетками и фибробластами. Узелки и васкулит могут также развиваться во многих органах.
Симптомы и признаки при ревматоидном артрите
Заболевание обычно развивается постепенно, начинаясь с системных симптомов и прогрессируя до суставных проявлений, но развитие этих двух групп признаков может наблюдаться и одновременно. Системные проявления включают утреннюю скованность пораженных суставов, общую дневную утомляемость и недомогание, потерю аппетита, общую слабость и субфебрильную температуру тела. Суставные симптомы включают боль и скованность.
Характерна симметричность поражения суставов. В типичных случаях скованность длится больше 60 минут по утрам, но может наблюдаться и после любого длительного периода отсутствия активности. Пораженные суставы становятся болезненными, гиперемированными, горячими на ощупь, отечными; ограничивается объем движений в них. Запястья и пястнофаланговые суставы указательного и среднего пальцев поражаются наиболее часто, несколько реже — проксимальные межфаланговые и плюснефаланговые, локтевые и голеностопные суставы; тем не менее поражаться могут любые суставы. Часто вовлекается в процесс осевой скелет. Определяется также утолщение синовиальной оболочки. Суставы часто находятся в состоянии сгибания для минимизации боли, которая возникает в результате растяжения суставной капсулы.
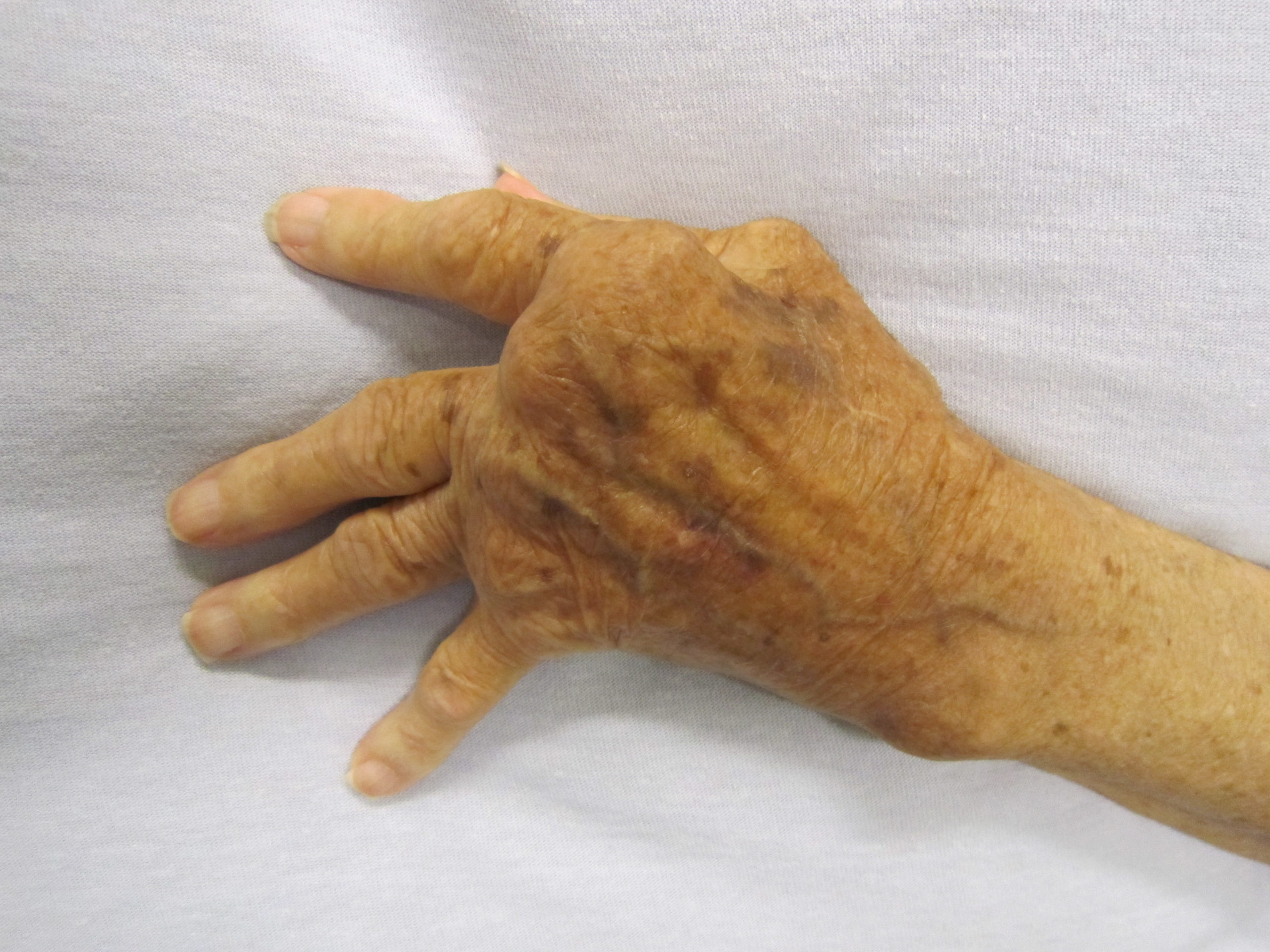
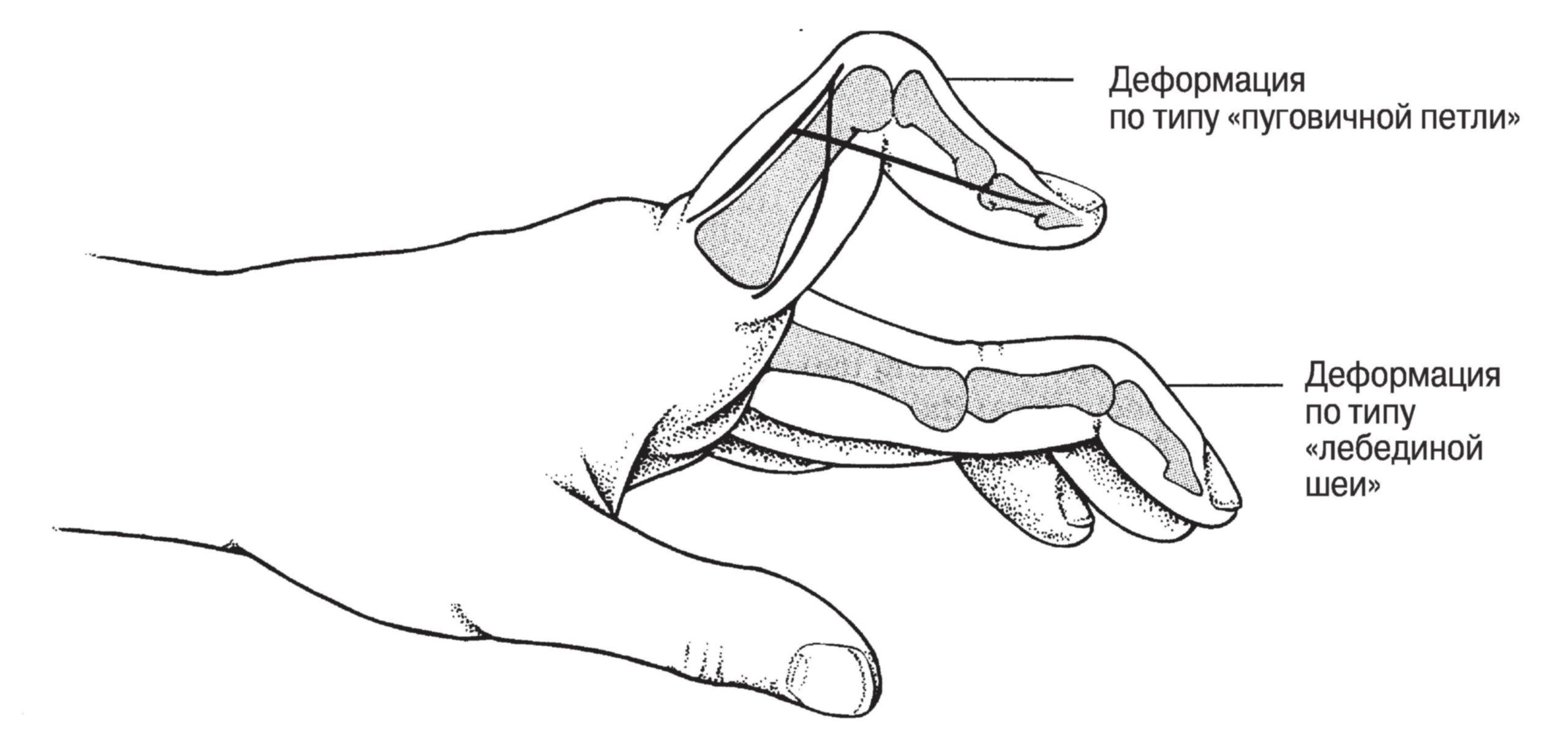
Деформации, особенно сгибательные контрактуры, развиваются быстро; типична ульнарная девиация пальцев с локтевым смещением сухожилий разгибателей с тыльной поверхности пястнофаланговых суставов, а также деформации по типу «шеи лебедя» и «пуговичной петли» (см. рис. ниже).
Также имеет место нестабильность суставов. При синовите лучезапястногло сустава и сдавлении срединного нерва развивается туннельный синдром запястного канала. Возможны разрывы кисты Бейкера с развитием отеков и болей в области голени, что требует дифференциальной диагностики с тромбозом глубоких вен данной области.
Подкожные ревматоидные узелки — нечастая находка на ранних стадиях заболевания, однако впоследствии они развиваются более чем у 30 % больных, обычно в местах, подвергаемых давлению и раздражению (например, на разгибательной поверхности предплечья). Висцеральные узелки обычно бессимптомны и часто отмечаются при тяжелом течении ревматоидного артрита. Другими внесуставными проявлениями являются васкулит, вызывающий язвы нижних конечностей, множественный мононеврит, плевральный или перикардиальный выпот, очаговые образования легких, фиброз легких, перикардит, миокардит, лимфаденопатия, синдром Шегрена, эписклерит, спленомегалия, пигментные пятна на коже (в рамках синдрома Фелти). Поражение шейного отдела позвоночника может приводить к подвывиху в атлантоаксиальном суставе и компрессии спинного мозга; это может затруднить разгибание шеи (например, при проведении эндотрахеальной интубации).
Течение заболевания непредсказуемо. Наиболее быстро оно прогрессирует в течение первых 6 лет, особенно в первый год; у 80 % больных суставные поражения развиваются в течение 10 лет.
Диагностика
Ревматоидный артрит должен быть заподозрен у больных, предъявляющих жалобы на множественные симметричные поражения суставов. Критерии диагностики ревматоидного артрита перечислены в таблице ниже; наличие четырех и более критерпев является основанием для постановки диагноза. Пациентам должны быть выполнены исследования на наличие РФ, рентгенологическое исследование кистей и стоп; кроме того, следует провести рентгенографию пораженных суставов с целью оценки последующей динамики эрозивных изменений.
Таблица. Диагностика ревматоидного артрита1
| Для постановки диагноза ревматоидного артрита необходимо наличие у пациента любых четырех критериев: | |
| Утренняя скованность длительностью не менее 1 часа | |
| Поражение 3 и более суставов | |
| Артрит суставов кистей (запястных, плюснефаланговых или межфаланговых) | |
| Симметричный артрит | |
| Ревматоидные узелки | |
| Ревматоидный фактор в сыворотке крови (положителен менее чем у 5 % здоровых людей) | |
| Рентгенологические изменения (эрозии или неравномерный остеопороз костей на рентгенограммах кистей) | |
1 На основе критериев Американской ревматологической ассоциации (в настоящее время — Американской коллегии ревматологов).
РФ (представляющий собой антитела к человеческим гамма-глобулинам) выявляется приблизительно у 70 % больных. Тем не менее РФ, часто в низких титрах, может обнаруживаться и при других заболеваниях, включая заболевания соединительной ткани (например, СКВ), гранулематозы, хронические инфекции (например, вирусный гепатит, подострый бактериальный эндокардит, туберкулез), злокачественные новообразования. РФ в низких титрах также обнаруживается у 3 % представителей общей популяции и приблизительно у 20 % пожилых людей. Титр РФ в реакции латекс-агглютинации выше 1:80 подтверждает наличие ревматоидного артрита. В настоящее время оценка концентрации РФ проводится путем нефелометрии; нормальные значения могут варьировать в различных лабораториях.
Определение антицитруллиновых антител является высокоспецифичным (90 %) и чувствительным (96 %) признаком ревматоидного артрита, полезным при дифференциальной диагностике ранних полиартритов.
В первые месяцы болезни при рентгенографии отмечается только отек мягких тканей. Впоследствии наступают заметные изменения в виде остеопороза образующих сустав костей, сужения суставной щели и краевых эрозий. Часто эрозии развиваются в первый год заболевания, но могут отмечаться в любое время. Более чувствительным методом является МРТ, позволяющая выявить ранние признаки воспаления в суставе и эрозии.
При установленном диагнозе ревматоидный артрит дополнительные исследования полезны в выявлении осложнений. Необходимо выполнение общего анализа крови. Нормохромная (или несколько гипохромная) нормоцитарная анемия имеет место у 80 % пациентов; концентрация гемоглобина при этом обычно выше 10 г/дл. При снижении данного показателя до 10 г/дл и ниже, следует предположить присоединение железодефицитной анемии и провести поиск на предмет возможных ее причин. Нейтропения имеет место в 1—2 % случаев и часто сопровождается спленомегалией (синдром Фелти). Тромбоцитоз, повышение СОЭ и концентрации С-реактивного белка отражают активность заболевания. Имеет место невыраженная поликлональная гипергаммаглобулинемия. СОЭ повышена у 90 % больных в активной фазе; концентрация сывороточного комплемента — нормальная или повышенная.
Исследование синовиальной жидкости необходимо при любых вновь возникших артритах или появлении внутрисуставного выпота с целью дифференциальной диагностики ревматоидного артрита и артритов другой природы (например, септических или микрокристаллических). При ревматоидном артрите в стадии острого воспаления сустава синовиальная жидкость мутная, желтого цвета, стерильная, с низкой вязкостью и содержанием лейкоцитов в диапазоне от 10 000 до 50 000 клеток/мкл; обычно преобладают полиморфноядерные нейтрофилы, но более 50 % клеток могут быть представлены лимфоцитами и другими мононуклеарами. В цитоплазме лейкоцитов обнаруживаются включения, что может быть выявлено при исследовании нативного препарата. Кристаллы отсутствуют.
Дифференциальный диагноз
Многие заболевания клинически схожи с ревматоидным артритом. У многих больных микрокристаллическими артритами отмечается соответствие критериям ревматоидного артрита; однако анализ синовиальной жидкости в данном случае позволяет уточнить диагноз. Присутствие кристаллов делает диагноз ревматоидный артрит маловероятным. Как и при ревматоидном артрите, при подагре, холестеринозе и амилоидозе могут наблюдаться поражения суставов и подкожные узелки; в таких случаях необходима аспирационная или эксцизионная биопсия узелков.
При СКВ, в отличие от ревматоидного артрита, имеются кожные поражения на открытых участках тела, подвергаемых инсоляции, выпадение волос, поражение слизистых рта и носа. Характерно отсутствие эрозий суставных поверхностей даже при длительно текущих артритах, количество лейкоцитов в синовиальной жидкости составляет менее 2000 клеток/мкл (преимущественно мононуклеары), выявляются антитела к двуспиральной ДНК, поражение почек, низкие концентрации сывороточного комплемента. Артриты, подобные таковым при ревматоидном артрите, могут иметь место и при других заболеваниях соединительной ткани (например, полиартериите, склеродермии, дерматомиозите или полимиозите) либо могут отмечаться признаки нескольких заболеваний, что предполагает развитие смешанного заболевания соединительной ткани.
Суставы могут поражаться при саркоидозе, болезни Уиппла, множественном ретикулогистиоцитозе и других системных заболеваниях; в данном случае наличие специфических клинических признаков и биопсия ткани позволяют провести дифференциальную диагностику. В частности, при острой ревматической лихорадке поражение суставов носит мигрирующий характер и отмечается одновременно с нею, имеются указания на перенесенную ранее острую стрептококковую инфекцию (подтвержденные выделением культуры возбудителя или изменением титра антистрептолизина-О); напротив, при ревматоидном артрите проявления артрита обычно присоединяются к системным проявлениям позже.
Дифференциальная диагностика реактивных артритов возможна при наличии предшествующих проявлений со стороны желудочно-кишечного тракта или мочеполовой системы; кроме того, в данном случае отмечается асимметричное поражение суставов стопы, крестцово-подвздошных суставов и крупных суставов нижней конечности; а также развитие конъюнктивита, ирита, безболезненных изъязвлений слизистой щек, баланита или бленнорейной кератодермии на подошвах стоп и в других областях тела. Кроме того, часто отмечается повышение концентрации комплемента в сыворотке крови и суставной жидкости.
Псориатический артрит обычно асимметричен и редко ассоциируется с обнаружением РФ, но дифференциальная диагностика может быть сложной, особенно при отсутствии поражений кожи и ногтей. Однако в пользу данного диагноза свидетельствует вовлечение в процесс дистальных межфаланговых суставов и развитие тяжелого деструктивного артрита. Анкилозирующий спондилоартрит можно дифференцировать от ревматоидного артрита на основании поражения суставов позвоночника и осевых суставов, по отсутствию подкожных узелков и РФ.
Для остеоартрита характерно отсутствие ревматоидных узелков, системных проявлений РФ; в синовиальной жидкости количество лейкоцитов не превышает 2000 клеток/мкл.
Прогноз
Ревматоидный артрит снижает ожидаемую продолжительность жизни на 3—7 лет; при этом повышение летальности обусловлено поражением сердца, инфекциями, кровотечениями из желудочно-кишечного тракта; также негативное влияние могут оказывать агрессивная медикаментозная терапия, сопутствующие заболевания и развитие злокачественных новообразований.
Приблизительно у 10 % больных отмечается тяжелая инвалидизация, несмотря на проводимое адекватное лечение. Прогноз хуже у представителей европеоидной расы и женщин, при развитии подкожных узелков, манифестации заболевания в зрелом возрасте, наличии поражения 20 и более суставов, у продолжающих курить пациентов, а также при высоких значениях СОЭ и РФ.
Лечение ревматоидного артрита
Лечение включает сбалансированное сочетание покоя и физической нагрузки, адекватное питание, лечебную физкультуру и лекарственную терапию, в редких случаях — оперативные вмешательства.
Покой и питание. Полный покой (постельный режим), даже на короткое время, показан лишь в редких случаях; тем не менее необходимо рекомендовать пациентам регулярный отдых. Диета — обычная; в редких случаях у пациентов могут отмечаться обострения ревматоидного артрита после приема пищи; однако специфические пищевые продукты, ухудшающие течение ревматоидного артрита, неизвестны. Поэтому соблюдение определенной диеты нецелесообразно. Замещение -3-жирными кислотами (содержащимися в рыбьем жире) вместо -6-жирных кислот (содержащихся в мясе) может уменьшать выраженность проявлений заболевания за счет снижения продукции воспалительных простагландинов.
Лечебная физкультура. Иммобилизация пораженных суставов позволяет уменьшить выраженность воспаления и снизить выраженность клинических проявлений. Часто полезно ношение ортопедической или спортивной обуви с хорошей пяткой и наличием опоры для свода стопы; специальные вкладыши снижают интенсивность боли в плюснефаланговых суставах. Специальная обувь может понадобиться при развитии выраженных деформаций стоп. Ежедневное использование вспомогательных приспособлений может требоваться многим больным при инвалидизирующем течении ревматоидного артрита.
Лечебная физкультура должна проводиться осторожно. При остром воспалении выполнение пассивных движений помогает предотвратить развитие сгибательных контрактур. После стихания воспаления следует приступать к активным физическим упражнениям, проведение которых предотвращает развитие контрактур и сохранения мышечной силы. Активные упражнения (включающие прогулки и специальные упражнения для пораженных суставов) способствуют сохранению мышечной массы и объема движений в суставах, но не должны быть изнурительными. Сгибательные контрактуры могут потребовать интенсивной лечебной физкультуры, использования специальных корригирующих лонгет или иммобилизации в разогнутом положении. Парафиновые ванны облегчают выполнение упражнений для кистей и стоп.
Хирургические вмешательства. Вопрос о необходимости хирургических вмешательств должен рассматриваться с учетом общей картины заболевания. Например, при деформациях кистей и верхних конечностей, ограничивающих возможности использования костылей при реабилитации; при выраженных поражениях коленных суставов и стоп, ограничивающих эффективность хирургических вмешательств на тазобедренных суставах. Для каждого пациента должны быть определены индивидуальные показания с учетом функциональных характеристик. Хирургическое лечение может проводиться и во время активной фазы заболевания.
Эндопротезирование суставов показано при значительном нарушении их функции; наиболее успешно подвергаются протезированию тазобедренный и коленный суставы. Пациенты, перенесшие протезирование данных суставов, должны исключить значительные нагрузки (например, участие в профессиональных соревнованиях). Выполнение артродеза шейного отдела позвоночника может потребоваться при развитии компрессии спинного мозга. Резекция плюснефаланговых суставов, находящихся в состоянии подвывиха, может существенно облегчить ходьбу. Артродез суставов большого пальца кисти увеличивает силу пальцевого захвата. Артроскопическая или открытая синовэктомия может временно устранить воспаление в суставе.
Лекарственные средства, используемые при лечении ревматоидного артрита
Целью лечения является уменьшение выраженности воспаления, профилактика развития эрозий и прогрессирования деформаций. Противоревматические препараты, модифицирующие течение заболевания, начинают использоваться рано, часто в комбинации. Существует большое количество новых средств, замедляющих прогрессирование заболевания. НПВП способствуют снижению выраженности болевого синдрома при ревматоидном артрите, но не предотвращают развития эрозий и прогрессирования заболевания. Иногда при выраженном полиартрите их комбинируют с глюкокортикоидами. Внутрисуставное введение депо-форм глюкокортикоидов позволяет контролировать не только тяжелый моноартрит, но и олигоартриты.
НПВП. Аспирин более не используется при ревматоидном артрите, поскольку эффективные его дозы часто токсичны. Не следует комбинировать различные НПВП (см. таблицу), хотя некоторые больные могут получать параллельно аспирин в дозе <325 мг/суг в качестве антиагрегантной терапии. Поскольку максимальный эффект НПВП может развиваться в течение 2 недель, дозу препарата не следует повышать до истечения данного срока. Дозы препаратов, позволяющих гибкое дозирование, могут повышаться до достижения максимального клинического эффекта или максимальной рекомендуемой дозы.
Таблица. Нестероидные противовоспалительные средства, используемые при лечении ревматоидного артрита
|
Препарат |
Обычная доза (внутрь) |
Максимальная рекомендованная суточная доза |
|---|---|---|
|
Неселективные |
||
|
Диклофенак |
75 мг дважды в день или 50 мг трижды в день 100 мг один раз в день (с замедленным высвобождением) |
150 мг |
|
Этодолак |
300-500 мг дважды в день |
1200 мг |
|
Фенопрофен |
300-600 мг 4 раза в день |
3200 мг |
|
Флурбипрофен |
по 100 мг 2-3 раза в день |
300 мг |
|
Ибупрофен |
400-800 мг 4 раза в день |
3200 мг |
|
Индометацин |
25 мг 3-4 раза в день 75 мг два раза в день (с замедленным высвобождением) |
200 мг |
|
Кетопрофен |
50-75 мг четыре раза в день 200 мг один раз в день (с замедленным высвобождением) |
300 мг |
|
Меклофенамат |
50 мг 3-4 раза в день |
400 мг |
|
Набуметон |
1000-2000 мг/день за один или несколько приемов |
2000 мг |
|
Напроксен |
250-500 мг два раза в день |
1500 мг |
|
Оксапрозин |
1200 мг один раз в день |
1800 мг |
|
Пироксикам |
20 мг 1 р/д |
20 мг |
|
Сулиндак |
150-200 мг 2 раза в день |
400 мг |
|
Толметин |
По 400 мг три раза в день |
1800 мг |
|
Селективные ингибиторы ЦОГ-2 |
||
|
Целекоксиб |
200 мг один или два раза в день |
400 мг |
|
Мелоксикам |
7,5 мг 1 раз в день |
15 мг |
|
*ЦОГ-2 селективность для этого препарата не определена |
||
|
ЦОГ=циклооксигеназа |
||
НПВП могут вызывать пептические язвы и кровотечения из желудочно-кишечного тракта. Поэтому применение этих препаратов противопоказано при язвенной болезни желудка и двенадцатиперстной кишки. Другими возможными побочными эффектами данных средств являются головная боль, спутанность сознания и другие нарушения со стороны ЦНС, утяжеление артериальной гипертензии, отеки и снижение агрегации тромбоцитов. Возможно повышение концентрации креатинина в крови вследствие ингибирования синтеза простагландинов почками. Несколько реже отмечается развитие интерстициального нефрита. У больных крапивницей, ринитом или бронхиальной астмой, индуцированными приемом аспирина, аналогичная симптоматика может развиваться и при приеме других НПВП. Имеются сообщения о развитии агранулоцитоза.
Механизм действия НПВП связан с ингибированием фермента циклооксигеназы и снижением вследствие этого синтеза простагландинов. Некоторые проста-гландины, синтезируемые при участии ЦОГ-1, оказывают влияние на многие органы и системы организма (например, защищают слизистую желудка и ингибируют адгезию тромбоцитов). Синтез других простагландинов, индуцируемых при воспалении, контролируется ЦОГ-2. Селективные ингибиторы ЦОГ-2 (коксибы), например целекоксиб, равноэффективны неселективным НПВП, но обладают меньшим негативным влиянием на органы желудочно-кишечного тракта. В то же время убедительных данных об отсутствии у коксибов нефротоксичного эффекта не получено. Тем не менее недавние исследования показали, что некоторые коксибы повышают риск развития сердечнососудистой патологии (например, инфаркта миокарда, инсульта) при длительном их применении. Поэтому необходимо соблюдать осторожность при длительном применении данных препаратов и назначении их больным, имеющим факторы риска сердечно-сосудистой патологии.
Противоревматические средства, модифицирующие течение заболевания. Препараты этой группы замедляют прогрессирование ревматоидного артрита и показаны практически всем больным с данной патологией. Они отличаются друг от друга по химическому строению и фармакологическим свойствам. Для большинства препаратов для развития эффекта требуется от нескольких недель до нескольких месяцев. Приблизительно у двух третей пациентов наступает улучшение, но полная ремиссия развивается не всегда. Многие приводят к снижению активности заболевания (например, уменьшению СОЭ или эрозий по данным рентгенографии). Данные препараты обладают лишь минимальным непосредственным анальгетическим эффектом, поэтому часто необходимо комбинировать их с НПВП. Следует тщательно оценить риск применения данных препаратов и в дальнейшем проводить постоянный мониторинг их токсичности.
Комбинирование этих препаратов более эффективно, чем монотерапия. Например, комбинация гидрохлорохина, сульфасалазина и метотрексата превосходит по эффективности монотерапию метотрексатом или комбинацию двух других средств.
Метотрексат — антагонист фолиевой кислоты, обладающий иммуносупрес-сивным эффектом в высоких дозах. При лечении ревматоидного артрита используются противовоспалительные дозы. Препарат достаточно эффективен, и эффект его развивается относительно быстро (клиническое улучшение отмечается в течение 3—4 недель). Наиболее часто метотрексат используется перорально один раз в неделю, начиная с дозы 7,5 мг, которая постепенно повышается до необходимой (максимум — до 25 мг). Дозы выше 20 мг в неделю лучше вводить подкожно. Препарат следует использовать с осторожностью у пациентов, страдающих нарушениями функции печени и сахарным диабетом. Должен быть исключен прием алкоголя. Дозозависимый фиброз печени может развиваться внезапно, но обычно обратим. Возможно также угнетение костного мозга. В редких случаях встречаются пневмониты, однако они обычно фатальны. Могут также развиваться стоматиты и тошнота. Пероральный прием фолиевой кислоты в дозе 1 мг 1 раз в сутки может уменьшить выраженность токсических проявлений метотрексата. Каждые 6—8 недель следует выполнять общий анализ крови, определение активности ACT, АЛТ, щелочной фосфатазы, а также концентрации альбумина и креатинина. Выполнение биопсии печени может потребоваться при стойком повышении значений функциональных проб печени в 2 раза относительно верхней границы нормы и необходимости продолжения приема метотрексата. После отмены метотрексата может наблюдаться рецидив артрита.
Для лечения умеренно выраженного ревматоидного артрита также используется гидроксихлорохин. Токсические эффекты данного средства обычно умеренно выражены и включают дерматиты, миопатию, обычно обратимое помутнение роговицы. Тем не менее имеются сообщения о необратимой дегенерации сетчатки. До лечения и затем каждые 6—12 месяцев во время лечения следует проводить исследование полей зрения и фундоскопию. Препарат принимается перорально, начальная доза составляет 400 мг 1 раз в сутки (например, во время завтрака или обеда) в течение приблизительно 4—12 недель, затем снижается до 200 мг 1 раз в сутки. При отсутствии улучшения в течение 9 месяцев терапии необходима отмена препарата. Напротив, после достижения улучшения дозу снижают до поддерживающей, составляющей 200—400 мг 1 раз в сутки длительно.
Сульфасалазин может улучшить течение заболевания и замедлить развитие поражения суставов. Препарат обычно используется в виде таблеток, покрытых кишечнорастворимой оболочкой, начиная с дозы 500 мг (вечером), которая повышается путем дополнительного приема 500 мг (утром) и до 1000 мг (вечером), затем — 1000—1500 мг 2 раза в сутки. Клинический эффект достигается в течение 3 месяцев. Побочные эффекты могут включать проявления со стороны желудка, нейтропению, гемолиз, гепатит и кожные высыпания. Переносимость препарата улучшается при использовании его в виде таблеток, покрытых кишечнорастворимой оболочкой, или снижении дозы. Подсчет количества форменных элементов проводится через 2—4 недели после начала лечения, затем — каждые 12 недель на фоне продолжения терапии. Мониторинг активности ACT и АЛТ необходимо проводить каждые 6 месяцев, а также после любого повышения дозы.
Парентеральные препараты золота могут замедлить прогрессирование ревматоидного артрита. В последние годы их применение снизилось из-за токсичности и наличия более эффективных лекарств. Данные средства могут назначаться внутримышечно, в виде золота натрия тиомалата, с интервалом в 1 неделю, по схеме: 10 мг — в первую неделю, 25 мг — во вторую неделю, затем — 25—50 мг в неделю до достижения общей дозы в 1 г или значительного улучшения течения заболевания. После достижения максимального улучшения дозу снижают до 50 мг каждые 2—4 недели. Через 3—6 месяцев после прекращения лечения может наблюдаться рецидив. Однако часто достигается сохранение ремиссии в течение нескольких лет на фоне поддерживающей терапии. Ауранофин — препарат золота для перорального приема, назначаемый в дозах 3 мг 2 раза в сутки или 6 мг 1 раз в сутки.
Препараты золота противопоказаны при тяжелой патологии печени или почек или патологических изменениях клеточного состава крови. Наиболее частыми токсическими реакциями при использовании препаратов золота являются кожный зуд, дерматит, стоматит, альбуминурия в сочетании с нефротическим синдромом или без такового и угнетение костного мозга. Пероральный прием препаратов золота может приводить к усилению перистальтики кишечника. Токсические реакции требуют временной или постоянной отмены препаратов, в некоторых случаях необходимо применение глюкокортикоидов или хелатирующих средств.
Пероральный пеницилламин снижает выраженность проявлений заболевания и замедляет его прогрессирование. Тем не менее он используется редко из-за токсичности и недостаточной эффективности.
Глюкокортикоиды. Системные глюкокортикоиды снижают выраженность проявлений заболевания быстрее и в большей степени, нежели другие средства. Они так же, как предполагается, могут замедлять эрозирование кости. Тем не менее они не предотвращают деструкции суставов, и их клиническая эффективность со временем снижается. Более того, при отмене глюкокортикоидов может наблюдаться тяжелое обострение заболевания. Поскольку данный класс средств характеризуется долгосрочными побочными эффектами, многие врачи рекомендуют использовать их только после оценки эффективности других средств.
Глюкокортикоиды могут быть полезны при выраженных суставных или системных проявлениях ревматоидного артрита (например, васкулите, плеврите или перикардите). Обычно доза преднизолона при пероральном приеме не должна превышать 7,5 мг/сут, за исключением пациентов, имеющих выраженные системные проявления заболевания. Не рекомендуется использование высоких нагрузочных доз глюкокортикоидов с их быстрым последующим снижением, равно как и прием препарата через день, поскольку в дни отсутствия приема глюкокортикоидов выраженность проявлений ревматоидного артрита значительно усиливается. Относительными противопоказаниями к назначению глюкокортикоидов являются пептические язвы, артериальная гипертензия, сахарный диабет, активные инфекции и глаукома. Перед назначением глюкокортикоидов должен быть оценен риск развития туберкулеза.
Внутрисуставное введение депо-форм глюкокортикоидов может временно облегчить боль и отек в одном или двух особенно болезненных суставах. Триамцинолона гексацетонид подавляет воспаление на наиболее длительное время; вводимая доза зависит от вида пораженного сустава (например, от 10 до 40 мг для коленного сустава). Также эффективны триамцинолона ацетонид и метилпреднизолона ацетат. Любой сустав не должен пунктироваться чаще, чем 3—4 раз в год, поскольку более частые пункции приводят к усилению деструктивных процессов. Так как вводимые эфиры глюкокортикоидов имеют кристаллическую структуру, примерно в 2 % случаев в первые несколько часов после инъекции местное воспаление может усиливаться. Хотя инфекции осложняют данную процедуру только в 1 случае из 40 000, их развитие необходимо заподозрить при сохранении боли в течение более чем 24 часов после инъекции.
Цитотоксические иммуносупрессивные средства. Лечение азатиоприном, циклоспорином или циклофосфамидом позволяет обеспечить эффект, аналогичный таковому при использовании модифицирующих течение заболевания противоревматических средств. В то же время иммуносупрессанты более токсичны, особенно циклофосфамид, который может вызывать миелосупрессию и повышать риск развития злокачественных новообразований. В результате эти препараты используются только у пациентов, не достигающих ответа на применение средств, модифицирующих течение заболевания, либо при необходимости снижения потребности в глюкокортикоидах. Лечение азатиоприном начинается с дозы приблизительно 1 мг/кг (50—100 мг) перорально 1—2 раза в сутки; доза может быть повышена на 0,5 мг/кг в сутки спустя 6—8 недель после оценки количества клеток крови, активности АЛТ и ACT, затем — с интервалом в 4 недели до максимальной дозы (2,5 мг/кг в сутки). Поддерживающая терапия проводится в минимальной эффективной дозе. Низкие дозы циклоспорина могут быть также эффективны как в монотерапии, так и в комбинации с метотрексатом, при возможно меньшей токсичности, нежели азатиоприн или циклофосфамид. Стандартная доза — перорально 50 мг 2 раза в сутки, но для минимизации токсичного влияния на артериальное давление, почки и желудочно-кишечный тракт не должна превышать 1,75 мг/кг 2 раза в сутки.
Новые лекарственные средства. Лефлуномид взаимодействует с ферментом, участвующим в метаболизме пиримидина. Его эффективность сопоставима с таковой метотрексата, но он обладает меньшим миелосупрессивным эффектом и реже приводит к развитию пневмонита. Лефлуномид может использоваться в комбинации с метотрексатом. Стандартная доза составляет 20 мг 1 раз в сутки (при развитии нежелательных эффектов — 10 мг 1 раз в сутки). Основные побочные эффекты — кожные реакции и нарушение функции печени. Анакинра является рекомбинантным антагонистом рецепторов ИЛ-1, принимающим участие в патогенезе ревматоидного артрита. Анакинра вводится подкожно в дозе 100 мг 1 раз сутки. Наиболее частыми нежелательными реакциями являются осложнения в месте введения, инфекции и лейкопения.
Антагонисты ФНО-а также используются при лечении ревматоидного артрита, замедляя прогрессирование эрозий и снижая количество новых эрозий. Хотя ответ на терапию развивается не всегда, многие пациенты отмечают улучшение, иногда уже после первой инъекции. Этанерцепт вводится подкожно в дозе 25 мг 2 раза в неделю. Инфликсимаб вводится внутривенно ка-пельно в дозе 3 мг/кг разведенным раствором натрия хлорида в день начала лечения, затем — через 2 и 6 недель, далее — с интервалом в 8 недель.
Адалимумаб вводится подкожно в дозе 40 мг каждые 2 недели. Хотя существуют определенные различия между этими препаратами, наиболее серьезной проблемой их использования являются инфекционные осложнения, в частности реактивация туберкулеза. Поэтому перед началом терапии необходимо проведение обследования пациентов на наличие туберкулеза путем выполнения рентгенографии или туберкулиновой пробы. К другим потенциальным побочным реакциям относятся нарушение функции печени, развитие лимфом, появление антиядерных антител, сопровождающееся развитием СКВ или без таковой, цитопении и демиелинизирующие заболевания нервной системы. Данные средства не должны использоваться у больных, страдающих заболеваниями коронарных артерий или сердечной недостаточностью. Этанерцепт, инфликсимаб и адалимумаб могут и, вероятно, должны использоваться в комбинации с метотрексатом.








































Odnoklassniki
VKontakte
Telegram
RSS