Все статьи с тегом "Немелкоклеточный рак легкого"
-
Лекарственные средства и препараты, медицинское оборудованиеПрепарат Алектиниб компании Roche показывает положительные результаты в III фазе клинического исследования для людей с ALK -положительным раком легкого на ранней стадии
Данные исследования ALINA, основанные на долгосрочных положительных результатах лечения поздних стадий заболевания, демонстрируют, что алектиниб («Алеценза») снижает...
«PRO Здоровье» 01.09.2023 -
ЗависимостьОтказ от курения следует включить в клинические рекомендации по лечению рака легкого
Тема курения и его влияния на выживаемость, прогноз и эффективность лечения онкологических больных очень актуальна и широко...
«PRO Здоровье» 30.01.2023 -
ЗаболеванияВ месяц борьбы с раком легкого – о новых возможностях терапии
Высокое бремя рака легкого требует непрерывной работы по созданию инновационной терапии и постоянной актуализации знаний о ней...
«PRO Здоровье» 18.11.2022 -
ЗависимостьОколо 70% случаев рака легкого в России диагностируют на III и IV стадиях
Рак легкого входит в тройку наиболее распространенных онкологических заболеваний в России, при этом почти у половины пациентов...
«PRO Здоровье» 11.10.2022 -
Лекарственные средства и препараты, медицинское оборудованиеКомбинация препаратов Опдиво (ниволумаб) и Ервой (ипилимумаб) в качестве терапии первой линии при неоперабельной злокачественной мезотелиоме плевры обеспечивала устойчивое повышение общей выживаемости через 3 года в сравнении с химиотерапией в исследовании III фазы CheckMate-743
Исследование CheckMate-743 является единственным исследованием III фазы, в котором было продемонстрировано увеличение общей выживаемости (теперь с периодом...
«PRO Здоровье» 21.09.2021 -
Лекарственные средства и препараты, медицинское оборудованиеPfizer объявила о регистрации препарата Лорвиква® (лорлатиниб) для терапии ALK+ распространенного рака легкого после прогрессирования на терапии первой или второй линии
Международная биофармацевтическая компания Pfizer объявила о регистрации в России нового препарата Лорвиква® (лорлатиниб) для терапии распространенного ALK+...
«PRO Здоровье» 10.09.2021 -
Психология и здоровьеОколо половины пациентов с раком легкого нуждаются в психологической поддержке
Почти половина пациентов с раком легкого (48,1%) испытывают острую потребность в психологической поддержке в процессе лечения. Как...
«PRO Здоровье» 06.09.2021 -
ЗаболеванияРезультаты длительного наблюдения подтверждают эффективность иммунотерапии для лечения немелкоклеточного рака легкого и плоскоклеточного рака головы и шеи
В рамках сателлитных симпозиумов компании MSD эксперты обсудили возможности применения комбинированной химио-иммунотерапии в 1 линии лечения пациентов...
«PRO Здоровье» 14.07.2021 -
Лекарственные средства и препараты, медицинское оборудованиеРегистрационное исследование III фазы показало, что атезолизумаб помогает определенным пациентам с операбельным раком легкого* жить значительно дольше, не беспокоясь о рецидиве
Атезолизумаб улучшает показатель выживаемости без рецидива заболевания более чем на треть у пациентов с PD-L1-позитивным операбельным раком...
«PRO Здоровье» 18.06.2021 -
Лекарственные средства и препараты, медицинское оборудованиеКомбинация препаратов дурвалумаб и тремелимумаб с химиотерапией показала преимущество по общей выживаемости терапии у ранее не получавших лечения пациентов с IV стадией немелкоклеточного рака легкого в исследовании POSEIDON
POSEIDON — исследование III фазы по оценке эффективности и безопасности применения препарата компании «АстраЗенека» дурвалумаб (антитело к...
«PRO Здоровье» 19.05.2021 -
Лекарственные средства и препараты, медицинское оборудование«АстраЗенека» запустила полный цикл производства препарата Тагриссо® (осимертиниб) в России
Тагриссо® (осимертиниб) – это лекарственный препарат, предназначенный для лечения пациентов с немелкоклеточным раком легкого (НМРЛ) при наличии...
«PRO Здоровье» 12.09.2020 -
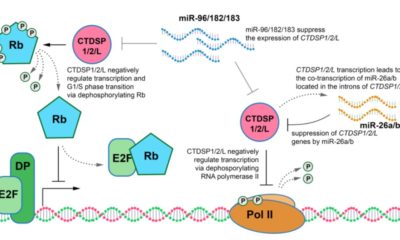
ЗаболеванияРоссийские исследователи предложили метод борьбы с одним из самых смертельных видов злокачественных опухолей
Российские исследователи предложили концепцию лечения немелкоклеточного рака легкого за счёт активации онкосупрессорной активности CTDSP-фосфатаз.
«PRO Здоровье» 15.07.2020 -
Лекарственные средства и препараты, медицинское оборудованиеКомпания «Рош» представила российским врачам новые данные клинических исследований своего онкологического портфеля
Завершился 6-й ежегодный международный онкологический форум «Белые ночи», который впервые проходил в онлайн формате.
«PRO Здоровье» 02.07.2020 -
Лекарственные средства и препараты, медицинское оборудованиеНа конференции ASCO «Рош» представит первые клинические данные о новом иммуноонкологическом препарате – антителе к TIGIT тираголумабу
В исследовании II фазы CITYSCAPE продемонстрированы многообещающие результаты применения комбинации тираголумаба и атезолизумаба у пациентов с PD-L1-позитивным...
«PRO Здоровье» 19.05.2020 -
Лекарственные средства и препараты, медицинское оборудованиеКомпания «Рош» подала заявку на регистрацию в России четырех новых показаний к применению атезолизумаба
В случае одобрения общее количество показаний к применению препарата достигнет 12-ти при шести типах злокачественных новообразований.
«PRO Здоровье» 28.04.2020 -
Лекарственные средства и препараты, медицинское оборудованиеFDA рассмотрит в приоритетном порядке заявку на атезолизумаб в качестве первой линии монотерапии при распространенном немелкоклеточном раке легкого
Ожидается, что решение по регистрации будет принято к 19 июня 2020 года.
«PRO Здоровье» 25.02.2020
-
УЗИ печени: когда проводится и для чего необходимоЗаболевания19.05.2022
-
НЕ обычная вода – почему стоит ввести в свой рацион минеральную воду «Ессентуки №4»Еда, продукты питания17.02.2021
-
Почему болит живот после еды?Еда, продукты питания30.09.2020
-
Ночные линзы для восстановления зрения — сколько стоят?Лекарственные средства и препараты, медицинское оборудование16.04.2022
-
«Ессентуки №4» и «Ессентуки №17» – особенности состава и применения легендарных минеральных водЕда, продукты питания11.03.2021
-
Причины возникновения и действия при биполярном расстройствеПсихология и здоровье23.10.2020
-
Уколы красоты: 10 самых популярных и эффективных инъекционных процедурКосметология19.05.2022
-
Чем полезен секс для женского здоровьяЛюбовь и отношения10.06.2022
-
Юбилейный ХХ съезд оториноларингологов России обозначил новые векторы развития специальностиНовости и пресс-релизы27.09.2021
-
Ступени жизни: открытие арт-объекта в поддержку пациентов с муковисцидозомЗаболевания06.07.2021
-
SuperJob: врачей перестали считать самой опасной профессией − рейтинг самых опасных профессийНовости и пресс-релизы29.04.2022
-
Возвращение легенды: Фенотропил® снова появится на прилавках аптекЛекарственные средства и препараты, медицинское оборудование26.05.2022
-
Когда можно мочить брови после перманентного макияжаКосметология22.12.2021
-
Около трети онкологических пациентов сталкиваются с психическими расстройствамиПсихология и здоровье31.05.2021
-
Инсульт можно предотвратить: простые шаги к здоровой жизниЗаболевания07.05.2025
-
Восстановление после родов: путь к здоровью молодой мамыБеременность07.05.2025
-
Ваше здоровье — ваша ответственность: путь к долголетию без мифовЗдоровый образ жизни07.05.2025
-
Длинные выходные и ресурс. Комментарий психологаПсихология и здоровье07.05.2025
-
5 основных причин снижения слуха: мнение отоларингологаЗаболевания07.05.2025
-
Дофаминовые прыжки: может ли новый тренд принести пользу здоровью? Мнение врачаЗдоровый образ жизни07.05.2025
-
Лишний вес: косметический недостаток или угроза здоровью?Заболевания06.05.2025
-
Почему родителям подростков важно перестать бояться психиатраПсихология и здоровье06.05.2025
-
Как подготовить себя к дачному сезону: советы гериатраПожилой возраст06.05.2025
-
Век здоровья: современные подходы к долголетиюБыть здоровым06.05.2025




























Odnoklassniki
VKontakte
Telegram
RSS